- 4 mars
Maladies inflammatoires chroniques de l’intestin : différences entre Crohn et rectocolite, symptômes, causes et rôle de l’alimentation
- Joris Vanlerberghe
- MICI : Crohn et Rectocolite
- 0 comments
Les maladies inflammatoires chroniques de l’intestin, souvent appelées MICI, regroupent principalement deux maladies : la maladie de Crohn et la rectocolite hémorragique.
Elles partagent un point commun central : une inflammation chronique de la paroi digestive, qui évolue par phases d’activité et de rémission. Mais elles diffèrent nettement par la localisation des lésions, la profondeur de l’inflammation, les symptômes dominants et le profil de complications.
Comprendre ces différences permet de mieux interpréter les symptômes, de mieux suivre l’activité inflammatoire, et d’adapter l’alimentation de façon pertinente, surtout quand l’objectif est double : limiter l’inconfort digestif tout en protégeant l’état nutritionnel.
1. Différences entre maladie de Crohn et rectocolite hémorragique
1.1 Où se situe l’inflammation
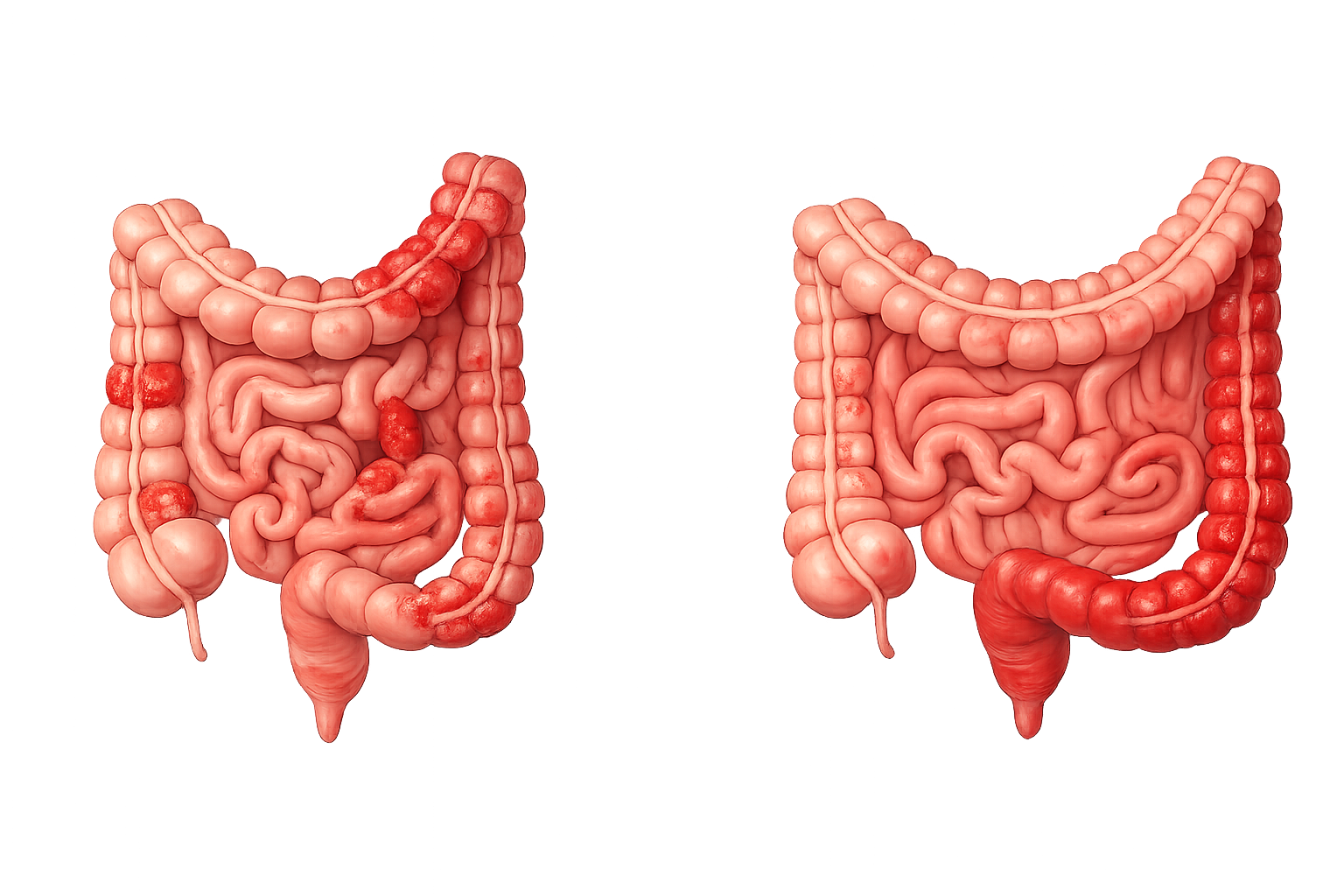
La maladie de Crohn peut toucher tout le tube digestif, de la bouche à l’anus. En pratique, les localisations les plus fréquentes sont l’iléon terminal et le côlon. L’atteinte est typiquement discontinue, avec alternance de segments atteints et de segments macroscopiquement normaux (comme l'image de gauche).
La rectocolite hémorragique touche uniquement le côlon et le rectum. L’inflammation commence presque toujours au niveau du rectum, puis s’étend de façon continue vers le côlon, sans “zones saines” intercalées (illustré avec l'image de droite).
Cette différence n’est pas un détail. Elle explique pourquoi certaines personnes ont surtout des urgences rectales et des saignements, alors que d’autres ont surtout des douleurs, des épisodes d’occlusion, ou des fistules.
1.2 La profondeur de l’inflammation change tout
Dans la rectocolite hémorragique, l’inflammation est essentiellement limitée à la muqueuse, parfois à la sous muqueuse. Cela veut dire que la couche superficielle qui tapisse l’intérieur du côlon est la plus touchée.
Dans la maladie de Crohn, l’inflammation est dite transmurale. Elle peut toucher toute l’épaisseur de la paroi intestinale. C’est ce caractère profond qui favorise des complications “mécaniques” comme les sténoses, les fistules et les abcès.
La conséquence concrète est simple.
Une rectocolite peut donner des diarrhées sanglantes et une muqueuse très fragile, mais beaucoup moins souvent des fistules.
Un Crohn peut donner des symptômes parfois moins “spectaculaires” sur les selles, mais avec un risque plus élevé de complications structurelles.
Sur ce point, les synthèses récentes rappellent bien l’importance des rétrécissement du calibre de l'intestin (à cause de l'inflammation) dans Crohn, qui concernent une proportion significative des patients au cours de l’évolution.
1.3 Lésions typiques et complications
Dans la rectocolite hémorragique, les symptômes et les complications sont souvent liés à une inflammation muqueuse diffuse.
On retrouve des rectorragies, une urgence défécatoire, du ténesme, une fréquence des selles augmentée, parfois un mégacôlon toxique lors des poussées graves, et à long terme un risque augmenté de dysplasie et de cancer colorectal selon la durée d’évolution et l’étendue de l’atteinte colique.
Dans Crohn, les complications sont davantage liées à la profondeur et au caractère segmentaire.
Une inflammation chronique transmurale favorise la fibrose, donc les sténoses. Elle peut aussi créer des trajets fistuleux vers d’autres segments digestifs, la peau ou des organes adjacents. Les abcès intra abdominaux font aussi partie des complications classiques. Les documents de consensus chirurgicaux et thérapeutiques insistent sur ces tableaux et sur l’articulation entre traitement médical et chirurgie selon le type de complication.
1.4 Différences immunologiques
Les deux maladies sont portées par des voies inflammatoires partiellement communes, dont le TNF alpha, mais aussi des voies plus spécifiques, notamment l’axe IL 12 IL 23, ce qui explique le développement de biothérapies ciblant ces voies dans Crohn et parfois dans la rectocolite selon les molécules.
Les recommandations sur les thérapeutiques dans Crohn rappellent la logique de ces cibles et la stratégie moderne centrée sur des objectifs mesurables comme la cicatrisation muqueuse.
2. Symptômes digestifs fréquents des MICI
2.1 Pourquoi les symptômes ne reflètent pas toujours l’inflammation
Une erreur fréquente est de penser que “plus j’ai mal, plus je suis inflammatoire”. C’est parfois vrai, mais pas toujours. Les symptômes digestifs dans les MICI proviennent de plusieurs mécanismes. Il y a l’inflammation elle-même, qui rend la muqueuse fragile, augmente la sécrétion, et stimule la motricité.
Il y a les complications mécaniques, comme une sténose ou un abcès, qui peuvent donner des douleurs intenses même si l’inflammation muqueuse n’est pas maximale au moment précis.
Il y a aussi des symptômes fonctionnels associés, type côlon irritable, qui peuvent persister en rémission inflammatoire.
C’est pour cela qu’on suit souvent l’activité avec des marqueurs comme la calprotectine fécale et l’endoscopie quand nécessaire, plutôt qu’uniquement sur le ressenti.
2.2 Les symptômes “classiques” en pratique
Dans la rectocolite hémorragique, la triade la plus typique associe
une diarrhée,
du sang dans les selles, et
une urgence défécatoire.
Le sang traduit l’ulcération muqueuse. L’urgence et le ténesme traduisent l’irritation rectale et la perte de capacité de rétention.
La fréquence peut varier de quelques selles au dessus du normal à des tableaux très sévères avec nombreuses selles sanglantes quotidiennes.
Dans la maladie de Crohn, les symptômes dominants dépendent de la localisation.
-
Quand l’iléon est touché :
douleurs de fosse iliaque droite,
une diarrhée parfois moins sanglante,
une perte de poids, et
des signes de malabsorption.
Quand le côlon est touché : les symptômes se rapproche parfois d’une rectocolite, mais le caractère discontinu et la profondeur des lésions modifient le risque de complications.
Les douleurs abdominales sont particulièrement fréquentes dans Crohn, notamment si une sténose se met en place. Dans ces cas, la douleur peut être post prandiale, associée à ballonnements, nausées, voire vomissements si l’obstacle est significatif.
2.3 Signes d’alarme digestifs
Certains symptômes sont des signaux qui doivent faire envisager une activité inflammatoire importante ou une complication.
Une fièvre, une douleur localisée intense, une masse abdominale, un amaigrissement rapide, des vomissements répétés, ou des douleurs anales importantes avec écoulements peuvent orienter vers un abcès, une fistule, ou une poussée sévère.
Dans la rectocolite, une distension abdominale avec douleur, fièvre et altération de l’état général fait évoquer un mégacôlon toxique, urgence médicale.
2.4 Manifestations extra digestives, très fréquentes
Même si votre demande cible le digestif, c’est utile de rappeler qu’une MICI est une maladie systémique.
Arthralgies,
spondylarthrite,
atteintes cutanées comme l’érythème noueux,
aphtes,
uvéites, et
atteintes hépato biliaires peuvent accompagner l’activité intestinale ou évoluer indépendamment.
Cela explique pourquoi l’évaluation globale d’un patient MICI ne se limite pas aux selles.
3. Causes et facteurs déclenchants
3.1 Le modèle scientifique actuel, simple et robuste
Le modèle le plus accepté est celui d’une maladie multifactorielle. Une prédisposition génétique augmente la susceptibilité. Des facteurs environnementaux modifient le microbiote, la barrière intestinale et l’immunité.
Le système immunitaire réagit de façon inappropriée à des signaux microbiens, entraînant une inflammation chronique.
Ce modèle est cohérent avec l’augmentation rapide des MICI dans les pays industrialisés et dans les pays en transition, ce qui est difficilement explicable par la génétique seule.
3.2 La part de la génétique, importante mais non suffisante
De nombreux loci génétiques associés aux MICI ont été identifiés. Certains concernent l’immunité innée, la reconnaissance bactérienne, l’autophagie et la barrière. Mais la génétique n’explique pas tout.
La concordance chez les jumeaux monozygotes est incomplète, ce qui confirme l’importance de l’environnement.
L’idée pratique est la suivante. On ne “choisit” pas de développer une MICI. Mais les expositions environnementales influencent fortement le risque et l’évolution.
3.3 Le microbiote, au coeur du problème mais pas en mode simpliste
Les MICI s’accompagnent d’une dysbiose. On observe souvent une baisse de diversité, une diminution de certaines bactéries productrices de butyrate, et une augmentation de bactéries potentiellement pro inflammatoires.
Cette dysbiose n’est pas seulement une conséquence.
Elle peut participer à l’entretien de l’inflammation en modifiant les métabolites disponibles, en perturbant le mucus, et en augmentant la translocation de composés bactériens.
Mais il faut rester précis. Le microbiote n’est pas une seule bactérie à “tuer”. C’est un écosystème à stabiliser.
Et les essais d’interventions ciblées microbiote ont des résultats variables, ce qui montre que le contexte inflammatoire et l’alimentation comptent autant que les souches.
3.4 La barrière intestinale et la perméabilité
La barrière intestinale est composée d’un mucus, d’une couche épithéliale, et de jonctions serrées.
Dans les MICI, ces éléments sont altérés. Une perméabilité accrue facilite le passage de fragments bactériens et alimentaires vers le compartiment immunitaire sous jacent.
L’immunité s’active, puis entretient à son tour les lésions de barrière. C’est un cercle vicieux.
Ce mécanisme aide à comprendre pourquoi certaines expositions alimentaires ou certains additifs peuvent théoriquement amplifier un terrain inflammatoire, surtout chez des sujets susceptibles.
3.5 Facteurs environnementaux associés au risque ou aux poussées
Le tabac est l’exemple le plus clair et le plus reproductible. Il augmente le risque de maladie de Crohn et aggrave son évolution. À l’inverse, il semble associé à un risque plus faible de rectocolite, mais cela ne signifie pas qu’il soit “protecteur” au sens clinique, car les effets cardiovasculaires et cancérogènes dépassent largement tout effet observé sur la rectocolite.
Les antibiotiques, surtout lorsqu’ils sont répétés ou précoces dans la vie, sont associés à un risque plus élevé de déséquilibre microbiote, donc potentiellement à une susceptibilité accrue.
Le stress n’est pas “la cause” au sens strict, mais il peut influencer les symptômes, la perméabilité, et certains marqueurs d’activité via l’axe cerveau intestin, ce qui peut favoriser des poussées chez certains patients.
L’environnement alimentaire moderne est un autre facteur majeur, surtout via la consommation d’aliments ultra transformés.
Plusieurs cohortes et analyses prospectives ont rapporté une association entre consommation élevée d’ultra transformés et risque accru de Crohn et de rectocolite, même si toutes les études ne sont pas parfaitement concordantes selon les pays et les méthodes de mesure.
Une revue récente, orientée sur les mécanismes des ultra transformés et additifs, discute aussi les voies plausibles, notamment via l’impact sur mucus, microbiote et perméabilité.
4. Le rôle de l’alimentation dans les MICI
4.1 Ce que l’alimentation fait, et ce qu’elle ne fait pas
L’alimentation ne remplace pas les traitements anti inflammatoires et immunomodulateurs quand ils sont indiqués.
Mais l’alimentation influence clairement quatre dimensions essentielles dans les MICI.
La charge symptomatique digestive : notamment les diarrhées, ballonnements, douleurs et urgences.
L’état nutritionnel : qui conditionne la fatigue, la masse musculaire, la tolérance aux traitements et la récupération.
Le microbiote et ses métabolites : qui peuvent moduler l’immunité intestinale.
L’exposition à certains composants potentiellement délétères sur la barrière chez des sujets sensibles, surtout en contexte inflammatoire.
Autrement dit, l’alimentation n’est pas un “traitement miracle”, mais c’est un levier réel, surtout si on l’utilise de manière ciblée et rationnelle.
4.2 Ultra transformés, additifs et risque inflammatoire
La littérature sur les aliments ultra transformés est en forte croissance. Des études prospectives ont retrouvé une association entre consommation élevée d’ultra transformés et risque accru de MICI. Les catégories impliquées varient, mais on retrouve souvent boissons sucrées, snacks, produits reconstitués, produits gras sucrés, et viandes transformées.
Sur le plan mécanistique, plusieurs hypothèses sont discutées.
La densité en sucres et graisses peut modifier les acides biliaires et l’écologie microbienne.
Certains additifs peuvent affecter le mucus ou la perméabilité dans des modèles expérimentaux.
Les émulsifiants, par exemple, sont fréquemment cités pour leur capacité à modifier la couche muqueuse et à favoriser une interaction plus proche entre bactéries et épithélium dans certains modèles. Il faut être rigoureux.
Les données mécanistiques ne signifient pas que “un additif déclenche à coup sûr une poussée”. Mais elles soutiennent une stratégie pragmatique.
Un article scientifique récent a montré un lien possible entre céréales raffinées et MICI.
Réduire les ultra transformés est cohérent avec les données de risque, cohérent avec les mécanismes plausibles, et globalement bénéfique pour la santé métabolique.
Dans la pratique clinique, c’est souvent l’un des changements les plus rentables, car il améliore la qualité globale du régime sans imposer une restriction extrême.
4.3 Fibres, fermentation et butyrate : bénéfice potentiel en rémission
Les fibres alimentaires ont un rôle central, surtout en rémission. Elles nourrissent le microbiote, augmentent la production d’acides gras à chaîne courte comme le butyrate, et soutiennent la santé de la muqueuse colique.
Le butyrate est souvent décrit comme un carburant des colonocytes et un modulateur immunitaire local. Cela plaide pour une alimentation riche en végétaux variés, quand la situation le permet. En phase active, ou en cas de sténose, certaines fibres insolubles et certains végétaux très irritants peuvent majorer la douleur ou le risque d’occlusion.
L’approche la plus solide consiste donc à raisonner en deux temps.
D’abord, sécuriser et soulager en poussée, parfois avec une réduction temporaire des résidus selon les symptômes et le risque sténosant.
Ensuite, reconstruire la diversité alimentaire en rémission, en réintroduisant progressivement des fibres tolérées.
4.4 Poussée inflammatoire : objectifs nutritionnels avant tout
En poussée, l’erreur la plus fréquente est de se concentrer uniquement sur “éviter ce qui fait mal”, au point de créer une dénutrition. Or la dénutrition est un facteur de mauvais pronostic, de fatigue chronique, et de mauvaise tolérance aux traitements.
Les objectifs prioritaires en phase active sont simples.
Assurer un apport énergétique suffisant. Assurer un apport protéique suffisant.
Limiter l’irritation mécanique si nécessaire, surtout en cas de sténose ou de diarrhée importante.
Corriger les déficits les plus fréquents.
Quand l’intestin est très inflammatoire, des aliments très riches en fibres insolubles, très gras, très épicés, alcoolisés ou très caféinés peuvent aggraver les symptômes chez certaines personnes. Cela ne prouve pas qu’ils aggravent la maladie au sens immunologique, mais cela peut dégrader le confort et l’hydratation.
Un régime de type “pauvre en résidus” peut être utile de façon transitoire dans certains contextes, mais il ne doit pas durer sans stratégie de réintroduction, car il appauvrit l’alimentation et peut réduire la production de métabolites protecteurs.
L'eau de coco a récemment démontré une capacité à réduire l'activité de la rectocolite hémorragique en combinaison avec les traitements médicamenteux.
Egalement, un régime basé sur la restriction du la production du sulfure d'hydrogène peut avoir un effet intéressant chez les malades de rectocolite hémorragique.
4.5 Nutrition entérale exclusive dans Crohn : un exemple fort de preuve
L’un des meilleurs exemples de stratégie nutritionnelle avec preuve d’efficacité anti inflammatoire est la nutrition entérale exclusive dans Crohn, surtout chez l’enfant.
Les recommandations et revues récentes rappellent qu’elle est considérée comme un traitement de première ligne pour induire une rémission dans Crohn pédiatrique, avec une efficacité notable et un impact sur la cicatrisation muqueuse.
Plusieurs mécanismes sont discutés :
réduction de l’exposition à certains composants alimentaires,
modulation du microbiote,
diminution d’antigènes,
effets directs sur la barrière.
Chez l’adulte, l’adhérence est plus difficile, et la place varie selon les pays, mais ce modèle montre une idée clé.
Dans Crohn, certaines interventions alimentaires peuvent agir au delà du simple “confort”, en influençant l’inflammation.
4.6 Régimes d’exclusion et approches structurées : prudence et nuance
Il existe des approches structurées comme des régimes d’exclusion spécifiques à Crohn, souvent combinés à une nutrition partielle. Certaines études suggèrent une amélioration clinique et parfois biologique, mais la qualité des preuves varie selon les protocoles, les populations et les critères de jugement.
Le point important pour un article destiné au grand public est de rester prudent. Une approche d’exclusion trop large augmente le risque de carences et de relation anxieuse à l’alimentation.
Le meilleur compromis est souvent une stratégie progressive et hiérarchisée.
Réduire les ultra transformés.
Travailler la qualité des apports, notamment protéines, oméga 3 alimentaires, variété végétale tolérée.
Adapter finement les fibres, les produits laitiers, les épices, les aliments très fermentescibles, en fonction des symptômes.
4.7 Et le régime pauvre en FODMAP dans les MICI
Le régime pauvre en FODMAP n’est pas un traitement de l’inflammation des MICI. Son intérêt est surtout symptomatique, chez des patients en rémission inflammatoire ou faible activité, qui gardent des symptômes fonctionnels de type côlon irritable, ballonnements, douleurs, diarrhée.
J'ai publié un article ici. Chez ces patients, réduire certains FODMAP peut diminuer gaz et distension, donc améliorer la qualité de vie.
Mais il faut insister sur deux points.
D’abord, il doit être temporaire et structuré, avec réintroduction, pour limiter l’appauvrissement du microbiote.
Ensuite, il ne doit pas retarder l’évaluation d’une poussée, car une aggravation des symptômes peut être inflammatoire.
4.8 Carences nutritionnelles fréquentes dans les MICI
Les MICI exposent à des carences par plusieurs mécanismes : pertes digestives, inflammation, malabsorption, restrictions alimentaires, chirurgie.
Les carences fréquentes incluent :
le fer, surtout dans la rectocolite avec saignements et dans Crohn colique.
La vitamine B12, surtout dans Crohn iléal et après résection iléale.
La vitamine D, dont le déficit est fréquent dans la population générale et encore plus dans les maladies inflammatoires chroniques.
Le zinc et le magnésium, plus variables selon diarrhées et apports.
Une alimentation “parfaitement tolérée” mais trop restrictive peut maintenir une fatigue majeure simplement par insuffisance d’apports et carences non corrigées.
4.9 Le régime méditerranéen : un socle intéressant en rémission
Quand l’objectif est de construire une base anti inflammatoire globale, sans tomber dans le régime strict, le régime méditerranéen est souvent un bon socle.
Il est riche en végétaux, en acides gras mono insaturés via l’huile d’olive, en poissons, en légumineuses, et pauvre en ultra transformés.
Il est associé à une réduction des marqueurs inflammatoires systémiques dans de nombreuses populations, et il est compatible avec une adaptation MICI, en ajustant les fibres et les textures selon la tolérance.
Cela permet de sortir de la logique “liste interdits”, tout en allant vers une alimentation cohérente avec la physiologie du microbiote.
4.10 Comment adapter concrètement, sans listes interminables
En poussée, l’idée n’est pas de “manger parfait”. L’idée est de limiter la contrainte mécanique et de sécuriser les apports. Textures plus faciles à digérer, cuisson douce, portions fractionnées, protéines digestes, féculents simples bien tolérés, hydratation. En rémission, l’idée est inverse.
Réintroduire progressivement la diversité.
Augmenter les végétaux tolérés,
Varier les sources de fibres,
Privilégier le fait maison,
Réduire les ultra transformés,
Reconstruire une relation alimentaire stable.
Si une sténose est connue ou suspectée, le niveau de prudence sur les fibres change totalement, et l’adaptation doit être médicale.
5. Quand consulter, et ce que la science considère comme objectifs modernes
Les objectifs actuels de prise en charge des MICI ne se limitent plus à “moins de symptômes”.
Les recommandations modernes visent une rémission plus profonde, souvent évaluée par la cicatrisation muqueuse et des biomarqueurs, car cela prédit un meilleur pronostic à long terme. La notion de cicatrisation muqueuse est devenue un objectif thérapeutique majeur, mais sa définition varie selon les essais et les scores utilisés, ce qui explique parfois des différences de résultats entre études.
Si les symptômes réapparaissent avec sang, fièvre, perte de poids, douleurs importantes, ou signes de complication, il faut une évaluation médicale rapide.
L’alimentation ne doit jamais retarder la prise en charge d’une poussée sévère.
Mon commentaire :
Dans la vraie vie, la majorité des personnes MICI se retrouvent coincées entre deux extrêmes.
D’un côté, on leur dit que l’alimentation “ne change rien”, ce qui est faux sur les symptômes, l’état nutritionnel et l’écosystème intestinal. De l’autre, elles tombent dans des régimes d’exclusion énormes, qui soulagent parfois sur le court terme, mais qui appauvrissent l’alimentation et entretiennent la peur de manger.
Le meilleur équilibre, selon mon expérience (et souffrant de rectocolite hémorragique moi-même), est presque toujours une stratégie en deux étages.
Un étage anti symptômes, court et ciblé.
Un étage de reconstruction, long et progressif, centré sur la diversité, la densité nutritionnelle et la réduction des ultra transformés.
L'erreur la plus souvent commise également par les malades de MICI est de penser que l'absence de symptôme = absence de maladie ou de crise. Or, la pathologie peut tout à fait est encore en phase active alors qu'il n'y a pas ou peu de symptômes. Une autre erreur consiste à ne pas prendre les médicaments de façon assidue, ce qui peut à termes favoriser une inflammation généralisée et l'escalade thérapeutique.
Références scientifiques
Magro F, Gionchetti P, Eliakim R, Ardizzone S, Armuzzi A, Barreiro-de Acosta M, Burisch J, Gecse KB, Hart AL, Hindryckx P, Langner C, Limdi JK, Pellino G, Zagórowicz E, Raine T, Harbord M, Rieder F; European Crohn’s and Colitis Organisation [ECCO]. Third European Evidence-based Consensus on Diagnosis and Management of Ulcerative Colitis. Part 1: Definitions, Diagnosis, Extra-intestinal Manifestations, Pregnancy, Cancer Surveillance, Surgery, and Ileo-anal Pouch Disorders. J Crohns Colitis. 2017 Jun 1;11(6):649-670. doi: 10.1093/ecco-jcc/jjx008. Erratum in: J Crohns Colitis. 2023 Jan 27;17(1):149. doi: 10.1093/ecco-jcc/jjac104. PMID: 28158501.
Ville A, McRae R, Nomchong J, Reidlinger DP, Davidson AR, Staudacher HM, Albarqouni L. Effects of a Low FODMAP Diet in Inflammatory Bowel Disease and Patient Experiences: A Mixed Methods Systematic Literature Review and Meta-Analysis. J Hum Nutr Diet. 2025 Aug;38(4):e70106. doi: 10.1111/jhn.70106. PMID: 40765115; PMCID: PMC12326053.
Lo CH, Khandpur N, Rossato SL, Lochhead P, Lopes EW, Burke KE, Richter JM, Song M, Ardisson Korat AV, Sun Q, Fung TT, Khalili H, Chan AT, Ananthakrishnan AN. Ultra-processed Foods and Risk of Crohn's Disease and Ulcerative Colitis: A Prospective Cohort Study. Clin Gastroenterol Hepatol. 2022 Jun;20(6):e1323-e1337. doi: 10.1016/j.cgh.2021.08.031. Epub 2021 Aug 28. PMID: 34461300; PMCID: PMC8882700.
Vissers E, Wellens J, Sabino J. Ultra-processed foods as a possible culprit for the rising prevalence of inflammatory bowel diseases. Front Med (Lausanne). 2022 Nov 7;9:1058373. doi: 10.3389/fmed.2022.1058373. PMID: 36419796; PMCID: PMC9676654.
Tita GVT, Serban DE, Chiperi LE, Fogas CR, Medan SA, Tantau VM. Exclusive enteral nutrition in Crohn's disease pediatric patients: from clinical remission to transmural healing. Med Pharm Rep. 2025 Jul;98(3):371-380. doi: 10.15386/mpr-2900. Epub 2025 Jul 30. PMID: 40786202; PMCID: PMC12334211.
Soublette Figuera A, Alessa S, Brien C, Hendrickson M, Kasvis P, Bessissow T. Effects of Ultra-Processed Foods and Food Additives on Disease Activity in Adults with Inflammatory Bowel Disease: A Scoping Review. J Clin Med. 2025 Nov 3;14(21):7798. doi: 10.3390/jcm14217798. PMID: 41227194; PMCID: PMC12608242.
À propos de l'auteur
Je suis Joris Vanlerberghe, naturopathe spécialisé dans les troubles digestifs et Auteur.
J’accompagne les personnes qui souffrent de troubles fonctionnels intestinaux comme le syndrome de l’intestin irritable (colopathie fonctionnelle), SIBO, IMO, dyspepsie ainsi que les personnes qui souffrent de maladies
inflammatoires chroniques intestinales : maladie de Crohn ou rectocolite hémorragique