- 5 août 2025
Régime FODMAP : amélioration de la perméabilité intestinale et mastocytes
- Joris Vanlerberghe
- Intestin irritable, FODMAP
- 0 comments
La prise en charge du syndrome de l’intestin irritable à prédominance diarrhéique (IBS-D) repose de plus en plus sur l’alimentation. Parmi les régimes les plus prometteurs, le régime pauvre en FODMAPs a démontré son efficacité symptomatique. Mais comment agit-il sur la barrière intestinale et le système immunitaire local ?
Une étude publiée en 2025 dans Gastroenterology vient bouleverser notre compréhension. Elle démontre que le régime FODMAP améliore la perméabilité intestinale et réduit l’activation des mastocytes, ces cellules clés de l’immunité intestinale. Voici un décryptage scientifique et vulgarisé de cette avancée majeure.
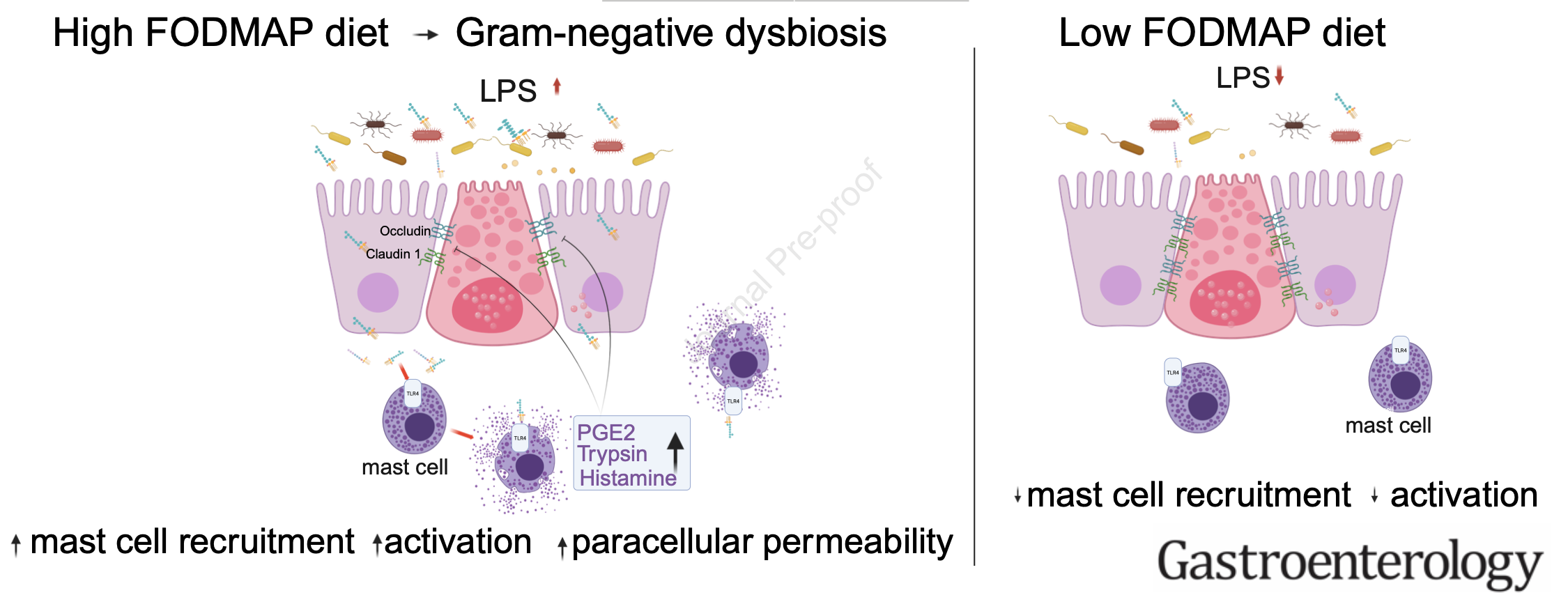
Les FODMAPs et leur impact physiologique
Les FODMAPs sont des glucides à chaîne courte fermentescibles : fructose, lactose, fructanes, galacto-oligosaccharides (GOS) et polyols. Ces substances ne sont pas bien absorbées dans l’intestin grêle chez de nombreuses personnes, et lorsqu'elles atteignent le côlon, elles subissent une fermentation rapide par le microbiote.
Cette fermentation produit des gaz (hydrogène, méthane, H2S) et augmente la charge osmotique, ce qui attire l’eau dans la lumière intestinale. Cette double action entraîne :
Ballonnements
Douleurs abdominales
Diarrhée ou alternance de transit
Cependant, leur rôle ne se limite pas à des effets mécaniques : les FODMAPs modifient aussi la composition microbienne, favorisant certains pathobiontes producteurs de lipopolysaccharides (LPS), une toxine bactérienne à fort potentiel inflammatoire.
Étude clinique : 42 patients IBS-D sous régime FODMAP strict pendant 4 semaines
Des chercheurs de l’université du Michigan et d’Harvard ont conduit une étude mécanistique rigoureuse. Quarante-deux patients atteints de SII-D ont suivi un régime FODMAP strict pendant 4 semaines.
Tous les repas étaient fournis par un service spécialisé, éliminant les biais d’observance.
L’étude a évalué :
La perméabilité intestinale (test lactulose/mannitol)
L’expression des protéines de jonction serrée (ZO-1, occludine, claudine-1…)
La densité et l’activité des mastocytes (histamine, PGE2, tryptase)
Les niveaux fécaux de LPS et la composition du microbiote
En parallèle, les chercheurs ont utilisé des modèles murins (souris) et des colonoïdes humains pour valider leurs hypothèses.
Renforcement objectif de la barrière intestinale
Chez les patients ayant répondu au régime (34/42), on observe :
Une augmentation de la TEER* (trans-epithelial electrical resistance)
Une augmentation des protéines de jonction serrée
Une baisse de l’excrétion urinaire du lactulose, marquant une meilleure étanchéité colique
La barrière intestinale est notre première ligne de défense contre les intrus : bactéries, toxines, LPS. Son intégrité est essentielle pour prévenir l’inflammation chronique.
*La TEER est une mesure directe de l’intégrité de la barrière intestinale, utilisée ex vivo sur des biopsies coliques ou des cultures cellulaires.
Si la TEER diminue :
Cela signifie que les jonctions serrées sont altérées
La perméabilité intestinale augmente
Des substances comme le LPS peuvent passer plus facilement dans la muqueuse
Si la TEER augmente :
La barrière intestinale est plus solide
Les cellules épithéliales sont plus soudées
C’est un signe de guérison ou de protection
Les mastocytes : sentinelles et saboteurs
Les mastocytes sont des cellules immunitaires présentes dans la muqueuse intestinale.
Leur rôle est double : détecter les menaces (LPS, antigènes alimentaires, stress) et réagir en libérant des médiateurs puissants :
Histamine : augmente la perméabilité vasculaire
Tryptase : dégrade les jonctions serrées
PGE2 : sensibilise les terminaisons nerveuses
Dans le SII-D, ces cellules sont souvent en surnombre, hyperactives et directement impliquées dans la douleur, la diarrhée et l’hypersensibilité viscérale.
Les tryptases : marqueurs clés de l’activation des mastocytes
Les tryptases sont des enzymes protéolytiques stockées dans les granules des mastocytes et libérées lors de leur activation. Elles jouent un rôle crucial dans la régulation de la perméabilité intestinale, car elles peuvent dégrader les protéines des jonctions serrées (comme ZO-1 ou occludine), contribuant ainsi à une altération de la barrière épithéliale.
Dans l’étude, les auteurs ont mesuré les niveaux de tryptase dans les biopsies coliques des patients atteints du SII-D avant et après le régime FODMAP.
Résultat : les patients répondeurs ont présenté une diminution significative des taux de tryptase, en parallèle d’une amélioration de la perméabilité intestinale.
Cela confirme que la réduction de l’activation mastocytaire, et donc de la libération de tryptase, est un mécanisme clé par lequel le régime FODMAP exerce ses effets bénéfiques.
PGE2 : médiateur pro-inflammatoire issu des mastocytes
La prostaglandine E2 (PGE2) est une molécule lipidique produite notamment par les mastocytes activés dans la muqueuse intestinale. Elle joue un rôle clé dans le développement de l’hypersensibilité viscérale, de la douleur abdominale et de l’inflammation silencieuse dans le SII-D.
La PGE2 peut également moduler la perméabilité épithéliale en affectant la signalisation intracellulaire des cellules de la barrière intestinale.
Dans l’étude de Gao et al. (2025), les niveaux de PGE2 dans les biopsies coliques ont été significativement réduits après 4 semaines de régime FODMAP, mais uniquement chez les patients répondeurs. Cette baisse est parallèle à celle de la tryptase et de l’histamine, et confirme que le régime FODMAP agit en partie en diminuant l’activation mastocytaire et ses effets sur l’épithélium.
Réduction de l’activation mastocytaire après le régime FODMAP
Après 4 semaines de régime FODMAP :
Le nombre de mastocytes diminue
Les taux de tryptase, histamine et PGE2 chutent
La correction de la barrière intestinale suit cette baisse d’inflammation
Ces modifications ne sont observées que chez les répondeurs. Le lien entre FODMAPs, mastocytes et inflammation est ainsi clairement établi.
Le rôle central du LPS et du récepteur TLR4
Le LPS (lipopolysaccharide), une molécule toxique présente à la surface des bactéries Gram-négatives, est reconnu par le récepteur TLR4, exprimé notamment sur les cellules épithéliales intestinales et certains mastocytes.
Cette interaction déclenche une réponse immunitaire innée via l’activation de la voie NF-κB, entraînant la production de cytokines pro-inflammatoires et de médiateurs comme la PGE2.
Dans certaines conditions, le LPS peut aussi contribuer à l’activation des mastocytes, provoquant la libération de tryptase et d’histamine, des molécules clés de l’inflammation et de la perméabilité intestinale.
L’étude montre que :
Le LPS est élevé dans les selles avant le régime
L’administration de ces selles à des souris entraîne une hyperperméabilité
Les souris TLR4-/- ou sans mastocytes ne présentent pas cette réaction
Le retrait du LPS ou son blocage abolit l’effet délétère
C’est la première fois qu’on démontre aussi clairement que le LPS fécal est un médiateur central dans l’atteinte de la barrière intestinale chez les SII-D.
Le TLR4 : pont entre microbiote et système immunitaire
Le récepteur TLR4 (Toll-Like Receptor 4) joue un rôle fondamental dans l’immunité innée. Il est chargé de reconnaître les motifs microbiens tels que le LPS et d’activer la cascade inflammatoire.
Dans un intestin sain, le TLR4 reste inactif, car la barrière empêche le LPS de l’atteindre.
En cas d’altération :
Le LPS traverse l’épithélium
Active le TLR4 des mastocytes
Déclenche la dégranulation et la production de cytokines
Aggrave la perméabilité, créant un cercle vicieux
Le régime FODMAP interrompt ce cycle en réduisant la source du LPS.
Diminution du LPS fécal après régime FODMAP
Les analyses montrent que :
Le LPS diminue fortement après 4 semaines
Cette baisse correspond à une diminution des bactéries Gram-négatives
On observe une corrélation positive avec les Bacteroidetes et une négative avec les Firmicutes
Bien que la diversité microbienne globale reste stable, les modifications ciblées suffisent à réduire le stress immunitaire local.
Expériences animales : confirmation du mécanisme
Les chercheurs ont validé leurs hypothèses sur plusieurs modèles :
Souris humanisées : les selles avant régime induisent la pathologie, celles d’après non.
Souris mastocyte-KO : protégées tant que non greffées avec mastocytes normaux.
Souris greffées TLR4-/- : insensibles au LPS fécal.
Ce protocole démontre que la boucle LPS → TLR4 → mastocyte → perméabilité est essentielle à la genèse des symptômes.
Comprendre la perméabilité intestinale
La barrière intestinale repose sur plusieurs couches :
Le mucus
L’épithélium (jonctions serrées, protéines ZO-1, occludine…)
Les cellules immunitaires sous-jacentes
Lorsque cette barrière est altérée :
Les molécules indésirables pénètrent
Le système immunitaire s’active (mastocytes, macrophages)
Un état inflammatoire de bas grade s’installe
La TEER, les tests au lactulose/mannitol et la microscopie des jonctions permettent d’évaluer cette perméabilité.
Un lien partiel avec l’amélioration clinique
Fait intéressant, la normalisation des paramètres biologiques ne prédit pas systématiquement une amélioration des symptômes. Cela suggère que :
D’autres facteurs contribuent aux douleurs SII : hypervigilance, anxiété, dysmotilité
Certains patients ont une barrière normale mais des symptômes exacerbés par le stress
L’effet placebo est élevé dans les essais SII (30 à 40 %)
Néanmoins, le régime FODMAP apporte une amélioration objective de l’inflammation muqueuse.
Les différents mécanismes pathologiques résumés



Cette étude valide une approche nutritionnelle ciblée et ouvre la voie à des stratégies thérapeutiques combinées, personnalisées, et basées sur des biomarqueurs.
Gao, J., Lee, A. A., Abtahi, S., Turner, J. R., Grover, M., Schmidt, A., Schmidt, T. M., Nee, J. W., Iturrino, J., Lembo, A., Chey, W. D., Wiley, J. W., & Singh, P. (2025). Low FODMAP diet improves colonic barrier function and mast cell activation in patients with IBS-D: A mechanistic trial. Gastroenterology. Advance online publication.
À propos de l'auteur
Je suis Joris Vanlerberghe, naturopathe spécialisé dans les troubles digestifs et Auteur.
J’accompagne les personnes qui souffrent de troubles fonctionnels intestinaux comme le syndrome de l’intestin irritable (colopathie fonctionnelle), SIBO, IMO, dyspepsie ainsi que les personnes qui souffrent de maladies
inflammatoires chroniques intestinales : maladie de Crohn ou rectocolite hémorragique