- 2 sept. 2025
Perméabilité intestinale : Crohn, cancer, inflammation ?
- Joris Vanlerberghe
- MICI : Crohn et Rectocolite
- 0 comments
La perméabilité intestinale, souvent appelée intestin perméable ou leaky gut, est au cœur de nombreux débats scientifiques. Longtemps cantonnée à un concept flou, elle est désormais reconnue comme un facteur clé dans l’évolution de plusieurs maladies chroniques. La barrière intestinale, composée de cellules épithéliales, de mucus et de protéines spécialisées comme les jonctions serrées, joue un rôle de filtre intelligent : elle laisse passer les nutriments essentiels tout en bloquant bactéries, toxines et antigènes alimentaires.
Lorsque ce mécanisme est altéré, la conséquence est une ouverture incontrôlée : bactéries et fragments alimentaires franchissent la paroi, déclenchant une inflammation chronique locale et systémique. Selon une revue publiée dans The Lancet Gastroenterology & Hepatology , cette dysfonction est impliquée dans les maladies inflammatoires chroniques de l’intestin (MICI) comme la maladie de Crohn et la rectocolite hémorragique, mais aussi dans le cancer colorectal, les maladies auto-immunes (polyarthrite rhumatoïde), et certaines atteintes neurodégénératives.
Dans cet article, nous explorerons les mécanismes scientifiques derrière la perméabilité intestinale, son lien avec Crohn, l’inflammation et le cancer, et les perspectives thérapeutiques actuelles.
Qu’est-ce que la perméabilité intestinale ?
La barrière intestinale est constituée :
d’un mur physique : cellules épithéliales reliées par des protéines de jonction (occludine, claudines, zonuline)
d’un mur chimique : mucus produit par les cellules caliciformes, peptides antimicrobiens, immunoglobulines (IgA)
d’un mur immunitaire : lymphocytes, macrophages, cytokines régulatrices
En temps normal, ces mécanismes assurent l’équilibre entre tolérance immunitaire et défense contre les pathogènes. Mais quand la régulation est perturbée, l’intestin devient « perméable ». Cette translocation bactérienne favorise la production de cytokines inflammatoires comme TNF-α, IL-17 ou IL-23, déclenchant une cascade inflammatoire qui ne se limite pas au tube digestif.
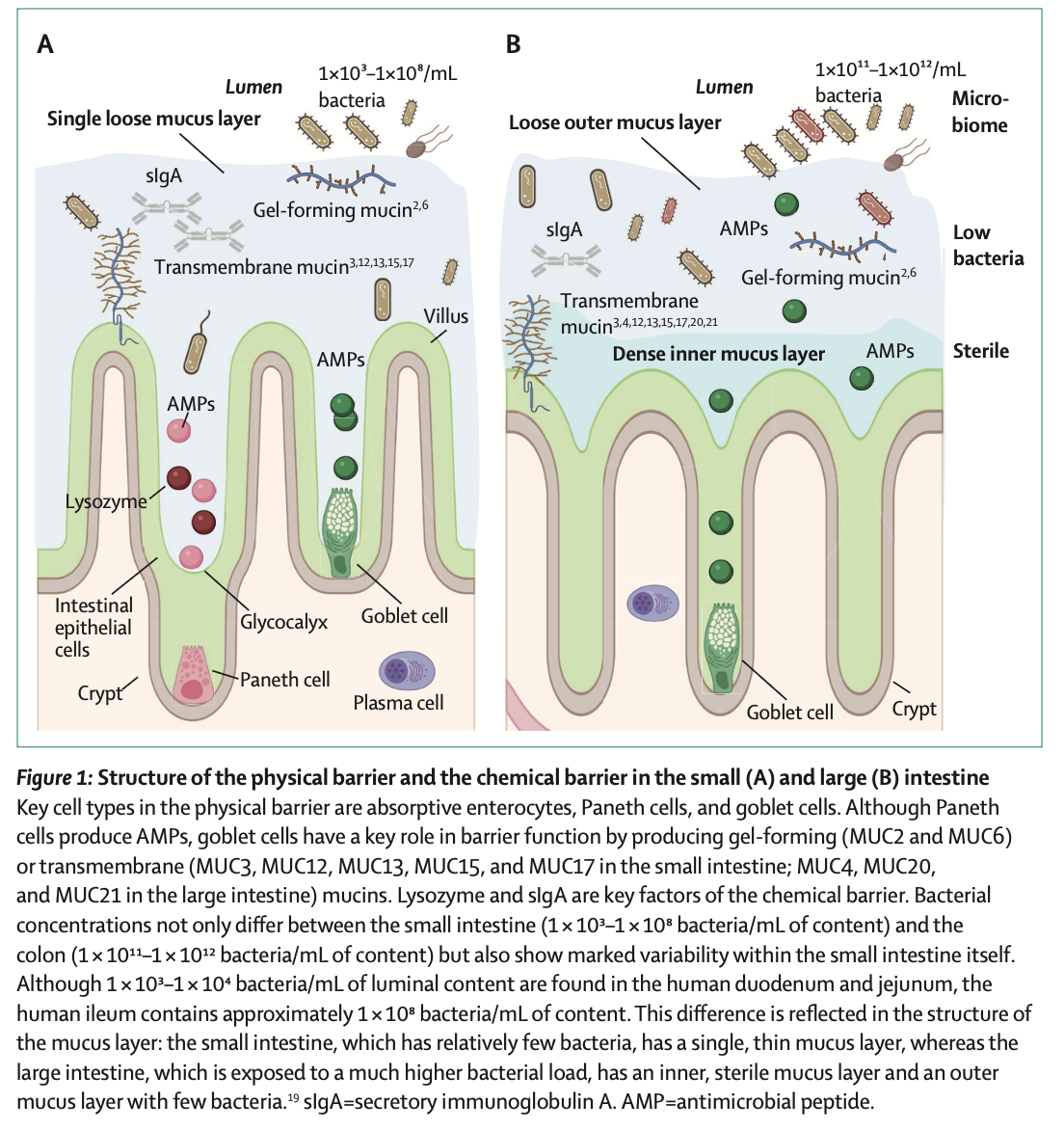
Image provenant de la revue The Lancet.
Perméabilité intestinale et maladie de Crohn
La maladie de Crohn est l’exemple le plus emblématique de l’implication du leaky gut. Les études montrent que la perméabilité intestinale est détectable jusqu’à trois ans avant l’apparition clinique de la maladie .
Les mécanismes en jeu :
Variants génétiques (NOD2, ATG16L1) altérant la capacité des cellules intestinales à gérer les bactéries
Diminution de la production de mucus (MUC2) et de peptides antimicrobiens par les cellules de Paneth
Dysbiose intestinale avec baisse de bactéries protectrices comme Faecalibacterium prausnitzii et hausse de pathobiontes comme Escherichia coli
Perturbations des jonctions serrées, notamment surexpression de claudin-2 qui favorise les fuites paracellulaires
Ces altérations conduisent à une inflammation chronique de la muqueuse digestive, avec formation d’ulcérations, d’abcès et de fistules.
Rectocolite hémorragique et altération de la barrière
La rectocolite hémorragique (RCH), autre grande MICI, est également marquée par une altération de la barrière :
Diminution des protéines de jonctions serrées (claudin-4, occludine)
Réduction du mucus protecteur produit par les cellules caliciformes
Présence accrue de bactéries pathogènes directement au contact de l’épithélium
La conséquence est une fragilité accrue de la muqueuse recto-colique, expliquant la survenue de saignements et d’ulcères. Là encore, la perméabilité intestinale n’est pas un simple épiphénomène, mais un moteur central de l’inflammation.
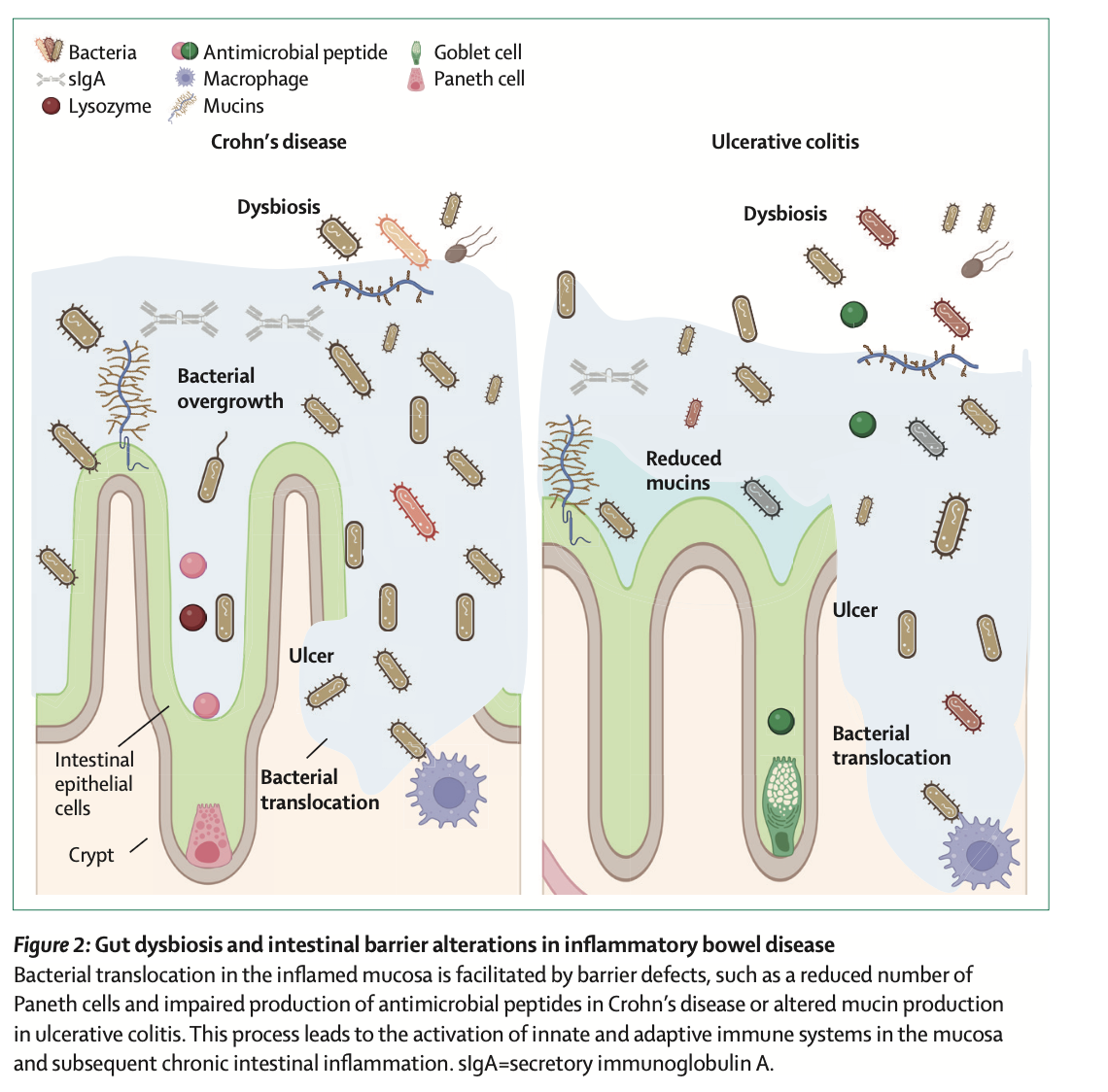
Image provenant de la revue The Lancet.
Perméabilité intestinale et cancer colorectal
Le cancer colorectal est aujourd’hui l’un des cancers les plus fréquents. Des altérations de la barrière intestinale apparaissent dès les phases précancéreuses.
Points clés :
Perte de mucus (MUC2) et baisse des protéines de jonction (JAM-A, claudines)
Translocation bactérienne favorisant la sécrétion de cytokines pro-tumorales (IL-23, IL-17A)
Présence accrue de bactéries oncogènes comme Fusobacterium nucleatum ou Bacteroides fragilis
Dysbiose intestinale aggravée par l’alimentation et l’obésité
La revue souligne que le microbiote joue un rôle direct dans la progression tumorale : certaines bactéries envahissent les tissus néoplasiques et créent un micro-environnement pro-inflammatoire qui stimule la croissance et la dissémination des cellules cancéreuses .
Le rôle du microbiote intestinal
La dysbiose intestinale est un élément central dans la perturbation de la perméabilité :
Perte de bactéries bénéfiques (productrices de butyrate)
Prolifération de bactéries pathogènes capables de dégrader le mucus
Production de métabolites délétères comme l’acide désoxycholique qui augmente la perméabilité
À l’inverse, certains métabolites comme le butyrate renforcent la barrière en stimulant la production de jonctions serrées et de mucus. Ce lien étroit entre microbiote et perméabilité explique l’intérêt croissant pour les probiotiques et prébiotiques dans les MICI et la prévention du cancer colorectal.
Cytokines et inflammation chronique
Les cytokines sont des médiateurs clés :
TNF-α : détruit les jonctions serrées et entretient l’inflammation (d’où l’efficacité des anti-TNF dans Crohn et RCH)
IL-17 et IL-23 : stimulent l’inflammation chronique et participent au développement du cancer colorectal
IFN-γ : induit la mort des cellules épithéliales et accentue les fuites de la barrière
IL-22 : au contraire, favorise la régénération de l’épithélium et la production de peptides antimicrobiens
L’équilibre entre cytokines pro-inflammatoires et régénératrices conditionne donc la santé intestinale.
La perméabilité intestinale au-delà des MICI
Le leaky gut n’est pas limité aux maladies digestives. La revue associe aussi une perméabilité augmentée à :
Polyarthrite rhumatoïde : via la translocation bactérienne et la citrullination des peptides
Stéatohépatite métabolique (NASH) et cholangite sclérosante primitive (PSC) : où des bactéries comme Klebsiella pneumoniae traversent la barrière et déclenchent une inflammation hépatique
Maladies neurodégénératives (Parkinson, Alzheimer) : l’hypothèse de l’axe intestin-cerveau s’appuie sur la circulation de cytokines et de fragments bactériens issus d’un intestin perméable
Ainsi, la perméabilité intestinale pourrait être un carrefour pathologique reliant inflammation intestinale, cancer et maladies systémiques.
Quelles solutions pour restaurer la barrière intestinale ?
Approches thérapeutiques actuelles et en développement :
Anti-TNF et anti-IL-23 : efficaces pour limiter l’inflammation dans Crohn et RCH
Inhibiteurs de la zonuline (AT-1001) : en essai, capables de réduire la perméabilité intestinale
Probiotiques ciblés (Lactobacillus rhamnosus GG, E. coli Nissle, Faecalibacterium prausnitzii) : renforcent les jonctions serrées et modulent la réponse immunitaire
Prébiotiques (fibres, amidon résistant) : favorisent la production de butyrate protecteur
Compléments nutritionnels : vitamine D (régule la production de claudines), acides gras polyinsaturés, polyphénols
Encapsulation de bactéries : nouvelle technologie permettant d’acheminer les probiotiques directement à la muqueuse intestinale
Ces approches, encore en cours d’évaluation, ouvrent la voie à une médecine personnalisée visant à restaurer la fonction barrière comme levier thérapeutique majeur.
Conclusion
La perméabilité intestinale est bien plus qu’un simple concept théorique. Elle représente un pivot biologiqueexpliquant l’émergence de maladies aussi diverses que la maladie de Crohn, la rectocolite hémorragique, le cancer colorectal ou encore certaines affections auto-immunes et neurodégénératives.
Comprendre les mécanismes qui fragilisent la barrière intestinale : dysbiose, cytokines inflammatoires, altération des jonctions serrées permet d’entrevoir de nouvelles pistes de traitement. Restaurer l’intégrité de l’intestin pourrait devenir une stratégie clé pour prévenir et soigner non seulement les MICI, mais aussi des pathologies systémiques où l’intestin joue un rôle caché mais fondamental.
À propos de l'auteur
Je suis Joris Vanlerberghe, naturopathe spécialisé dans les troubles digestifs et Auteur.
J’accompagne les personnes qui souffrent de troubles fonctionnels intestinaux comme le syndrome de l’intestin irritable (colopathie fonctionnelle), SIBO, IMO, dyspepsie ainsi que les personnes qui souffrent de maladies
inflammatoires chroniques intestinales : maladie de Crohn ou rectocolite hémorragique